新聞中心
相關(guān)資訊
咨詢熱線0551-62878850
據(jù)悉,北京科技大學(xué)的海明潭教授,上海交通大學(xué)附屬第六人民醫(yī)院朱悅琦主任和美國(guó)三院院士,哈佛大學(xué)的David A. Weitz教授通過(guò)微流控技術(shù)創(chuàng)建出了一種非常高效的納米給藥體系。通過(guò)這個(gè)納米藥物傳遞體系實(shí)現(xiàn)分子靶向藥物和化學(xué)藥物的多藥聯(lián)用,在低劑量靜脈注射的情況下,就可以抑制人類(lèi)表皮因子受體2陽(yáng)性乳腺腫瘤達(dá)到90%。這一******研究成果在線發(fā)表于知名學(xué)術(shù)期刊PNAS上。與傳統(tǒng)工藝相比,微流體技術(shù)可以極大的改善生產(chǎn)粒子的均一性,極大的提高藥物的裝載效率,并可以實(shí)現(xiàn)高通量的工業(yè)化生產(chǎn)。
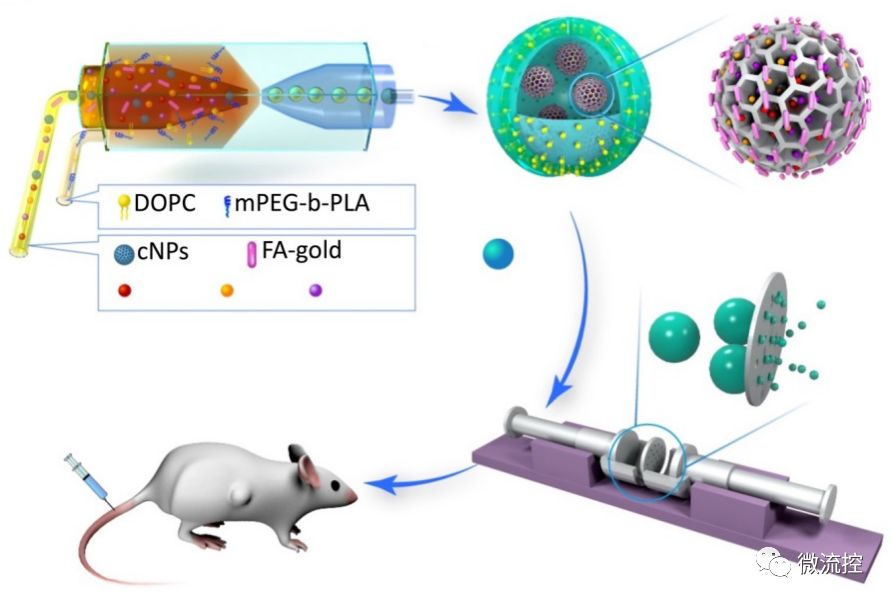
科研人員提出微流體雙乳體系,從而非常高效的實(shí)現(xiàn)封裝多種疏水性及親水性物質(zhì)。介孔硅納米粒子有非常好的生物相容性、生物可降解性、高載藥率及表面可功能化修飾等特點(diǎn)。而金納米粒子在生物成像及光熱治療方面被廣泛應(yīng)用。在該項(xiàng)目中,該研究團(tuán)隊(duì)首先把金納米棒通過(guò)化學(xué)反應(yīng)結(jié)合在介孔硅表面,然后通過(guò)介孔硅裝載大量親水、疏水、蛋白及核酸藥物,并通過(guò)微流體雙乳法一步將介孔硅包裹在了以高分子為主體,同時(shí)復(fù)合磷脂的巨型囊泡中。隨后,基于過(guò)膜擠壓的調(diào)控,構(gòu)建出了多藥物同時(shí)負(fù)載的納米載藥粒子。
該納米載藥體系在HER2陽(yáng)性乳腺癌小鼠模型中得到了驗(yàn)證。該納米體系有非常好的生物相容性,并可以在腫瘤中長(zhǎng)時(shí)間駐留。通過(guò)連續(xù)注射該納米體系,小鼠的腫瘤抑制率超過(guò)了90%,而且該體系極大的降低了癌細(xì)胞的耐藥性及藥物引起的副作用。
因?yàn)檫@個(gè)納米體系具有普適性,這個(gè)方法將有可能被廣泛應(yīng)用到其他類(lèi)型癌癥及其他類(lèi)型疾病的治療上。而且因?yàn)橹苽浞椒ê?jiǎn)單有效,研究團(tuán)隊(duì)認(rèn)為該方法有臨床轉(zhuǎn)化的潛力。希望研究團(tuán)隊(duì)帶來(lái)的納米載藥新體系,最終可以幫助更多癌癥患者改善預(yù)后。
本文轉(zhuǎn)自:電子發(fā)燒友網(wǎng),如有侵權(quán)聯(lián)系刪除